复旦团队揭示肺癌免疫治疗新靶点,为破解免疫抑制提供新思路!
| 导读 | 肺腺癌(LUAD)是癌症相关死亡的主要原因,肿瘤微环境(TME)在其发展过程中起着关键作用。 |
6月20日,复旦大学研究团队在期刊《Advanced Science》上发表了研究论文,题为“NDRG1-Driven Lactate Accumulation Promotes Lung Adenocarcinoma Progression Through the Induction of an Immunosuppressive Microenvironment”,本研究中,研究人员确定了 N-Myc 下游调节基因 1(NDRG1)是肺腺癌(LUAD)中的关键致病基因,与肿瘤进展和不良预后密切相关。机制研究表明,NDRG1 通过抑制乳酸脱氢酶 A(LDHA)的泛素化来稳定 LDHA,从而增强糖酵解并促进乳酸积累。这一过程通过诱导 M2 巨噬细胞极化、损害 CD8+ T 细胞功能以及上调免疫抑制基因来促进免疫抑制。此外,巨噬细胞中组蛋白 H3K18 乳酸化加剧了这种免疫抑制状态。临床上,NDRG1 表达升高与 PD-L1 水平升高、免疫抑制性巨噬细胞增多以及 CD8+ T 细胞浸润减少相关,导致免疫治疗耐药。相反,NDRG1 表达降低与 CD8+ T 细胞浸润增强以及治疗效果改善相关。临床前研究显示,靶向 NDRG1 可抑制肿瘤生长、减轻免疫抑制并增强抗 PD-L1 疗效。这些发现确立了 NDRG1 作为肺腺癌的关键调节因子和有前景的免疫治疗靶点。

https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202501238
背景知识
01
肺癌是全球最常见的恶性肿瘤之一,也是癌症相关死亡的主要原因。在肺癌中,肺腺癌是非小细胞肺癌(NSCLC)的主要亚型,近年来其治疗策略取得了显著进展。尽管手术、放疗和化疗等传统疗法有效,但在晚期或转移性肺腺癌的治疗中仍存在重大挑战。随着对肿瘤微环境(TME)认识的不断深入以及免疫疗法的出现,肺腺癌的治疗前景已从根本上得到改善。免疫疗法通过激活患者自身的免疫系统来识别并消灭癌细胞,已显示出显著提高患者生存率的潜力。此外,跨学科研究对于全面理解肺腺癌的复杂性和免疫逃逸机制、推动精准治疗策略的发展以及发现新的免疫治疗靶点以改善患者预后至关重要。
NDRG1 诱导的乳酸生成驱动免疫抑制功能
02
为了探究 NDRG1 诱导的乳酸生成在塑造免疫抑制性肿瘤微环境中的作用,研究人员开展了一系列实验。首先,研究人员发现 A549 细胞中 NDRG1 敲低显著降低了肿瘤条件培养基(TCM)中的乳酸水平。接下来,研究人员将这些巨噬细胞与 CD8⁺ T 细胞共培养 12 小时,以评估其免疫调节作用。研究显示 shNDRG1 组中髓源性抑制细胞(MDSCs)和 M2 巨噬细胞减少,同时 M1 样巨噬细胞和 CD8+T 细胞增加。
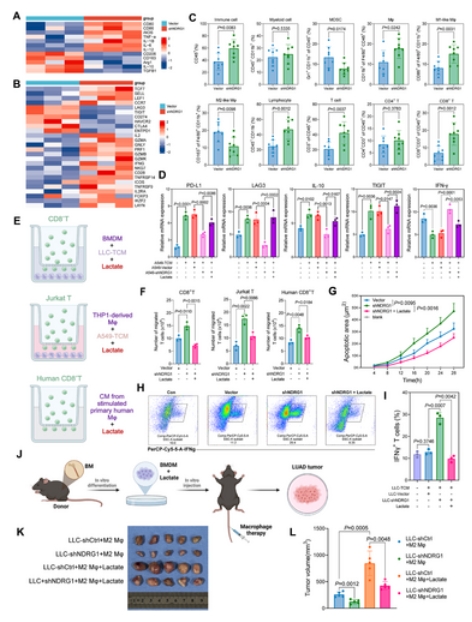
NDRG1 诱导的乳酸生成驱动免疫抑制
进一步的研究表明,NDRG1 通过促进乳酸积累来促进免疫抑制,这会调节对免疫功能至关重要的基因的表达。迁移和 T 细胞活化实验证实了这些发现。NDRG1 敲低增强了 CD8⁺ T 细胞和 Jurkat T 细胞的迁移和活化,而乳酸处理则逆转了这些效应。shNDRG1 组的肿瘤细胞凋亡显著增加,但这种增强作用部分被乳酸所抑制。同样,shNDRG1 提高了 IFNγ⁺ T 细胞的比例,而乳酸处理再次部分抑制了这一效应。
为了探究 NDRG1 诱导的乳酸生成在肿瘤进展中的作用,研究人员建立了一个皮下 LLC 肿瘤模型。LLC-shNDRG1+M2 巨噬细胞组的肿瘤明显小于 LLC-shCtrl+M2 巨噬细胞组,表明 NDRG1 敲低有效抑制了肿瘤生长。此外,在 LLC-shCtrl 和 LLC-shNDRG1 组中,乳酸处理的 M2 巨噬细胞与未处理的 M2 巨噬细胞相比,进一步促进了肿瘤进展。这些发现表明乳酸增强了 M2 巨噬细胞的促肿瘤活性。鉴于这些结果,研究人员提出乳酸可能诱导 M2 巨噬细胞发生乳酰化修饰,从而增强其免疫抑制活性并进一步推动肿瘤进展。
研究意义
03
本研究凸显了NDRG1 作为潜在治疗靶点的重要性,并强调了进一步研究以全面阐明其潜在机制和治疗潜力的必要性。(转化医学网360zhyx.com)
参考资料:
https://advanced.onlinelibrary.wiley.com/doi/10.1002/advs.202501238
【关于投稿】
转化医学网(360zhyx.com)是转化医学核心门户,旨在推动基础研究、临床诊疗和产业的发展,核心内容涵盖组学、检验、免疫、肿瘤、心血管、糖尿病等。如您有最新的研究内容发表,欢迎联系我们进行免费报道(公众号菜单栏-在线客服联系),我们的理念:内容创造价值,转化铸就未来!
转化医学网(360zhyx.com)发布的文章旨在介绍前沿医学研究进展,不能作为治疗方案使用;如需获得健康指导,请至正规医院就诊。
责任声明:本稿件如有错误之处,敬请联系转化医学网客服进行修改事宜!
微信号:zhuanhuayixue
 腾讯登录
腾讯登录









还没有人评论,赶快抢个沙发